https://sputniknewsbr.com.br/20211124/anvisa-autoriza-inclusao-de-dose-de-reforco-para-adultos-na-bula-da-pfizer-20260273.html
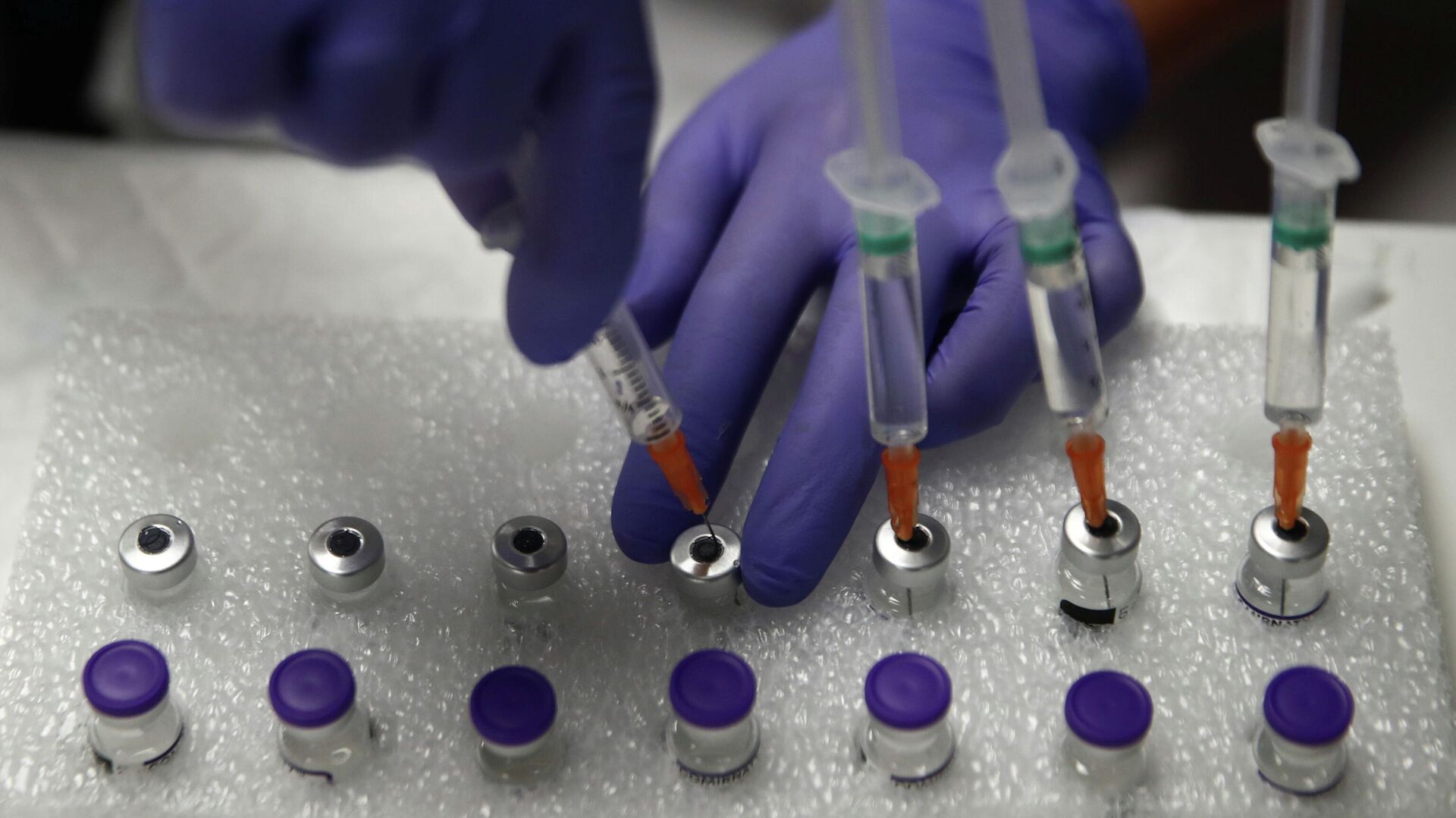
Anvisa autoriza inclusão de dose de reforço para adultos na bula da Pfizer
Anvisa autoriza inclusão de dose de reforço para adultos na bula da Pfizer
Sputnik Brasil
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quarta-feira (24), a autorização da dose de reforço solicitada pela Pfizer para a sua vacina... 24.11.2021, Sputnik Brasil
2021-11-24T18:34-0300
2021-11-24T18:34-0300
2022-02-14T10:24-0300
notícias do brasil
pandemia
vacinação
pfizer
covid-19
brasil vs. covid-19 em novembro de 2021
vacina
https://cdn1.sputniknewsbr.com.br/img/07e5/0b/18/20260432_0:321:3071:2048_1920x0_80_0_0_85ec3b32c0037c82284617333cb172d1.jpg
Com a autorização, a bula da vacina da Pfizer agora trará a indicação para a aplicação da dose de reforço pelo menos seis meses após o recebimento da segunda aplicação para pessoas com 18 anos ou mais.A decisão da Anvisa vale apenas para pessoas que receberam a própria vacina da Pfizer no ciclo vacinal.Apesar da aprovação, a agência ainda exige que a Pfizer firme um termo de compromisso para a apresentação de dados complementares identificados como lacunas durante a avaliação técnica.Os principais pontos do termo de compromisso, de acordo com a Anvisa, são: dados clínicos adicionais sobre eficácia; imunogenicidade e segurança da dose de reforço; plano de gerenciamento de risco com inclusão da dose de reforço; e dados de efetividade e de segurança de "vida real".
https://sputniknewsbr.com.br/20211124/sputnik-v-registra-80-de-eficacia-apos-8-meses-da-vacinacao-em-sao-marino-20255372.html
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
2021
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
notícias
br_BR
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
Sputnik Brasil
contato.br@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
pandemia, vacinação, pfizer, covid-19, brasil vs. covid-19 em novembro de 2021, vacina
pandemia, vacinação, pfizer, covid-19, brasil vs. covid-19 em novembro de 2021, vacina
Anvisa autoriza inclusão de dose de reforço para adultos na bula da Pfizer
18:34 24.11.2021 (atualizado: 10:24 14.02.2022) A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta quarta-feira (24), a autorização da dose de reforço solicitada pela Pfizer para a sua vacina contra a COVID-19. A agência concluiu que as evidências científicas demonstram segurança e eficácia para a aplicação da dose de reforço do imunizante.
Com a autorização, a bula da
vacina da Pfizer agora trará a indicação para a aplicação da dose de reforço
pelo menos seis meses após o
recebimento da segunda aplicação para pessoas com 18 anos ou mais.
A decisão da Anvisa vale apenas para pessoas que receberam a própria vacina da Pfizer no ciclo vacinal.
"A indicação de bula é baseada nos estudos clínicos e resultados desenvolvidos pelo laboratório, que neste caso avaliou a administração do reforço em voluntários que foram imunizados inicialmente com o esquema de duas doses da Pfizer",
explicou a Anvisa em nota.
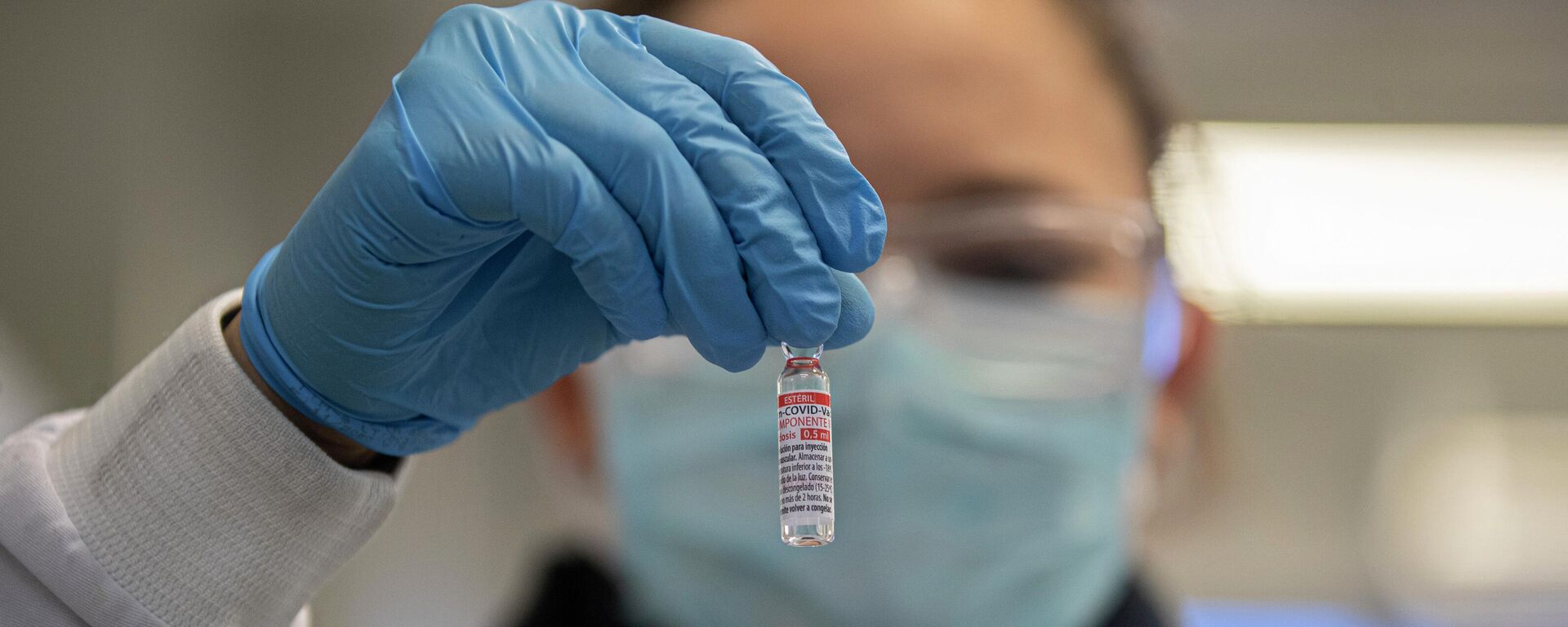
24 de novembro 2021, 13:29
Apesar da aprovação, a agência ainda exige que a Pfizer firme um termo de compromisso para a apresentação de dados complementares identificados como lacunas durante a avaliação técnica.
Os principais pontos do termo de compromisso, de acordo com a Anvisa, são:
dados clínicos adicionais sobre eficácia; imunogenicidade e segurança da dose de reforço; plano de gerenciamento de risco com inclusão da dose de reforço; e dados de efetividade e de segurança de "vida real".